สนใจทำการตลาดผ่านสื่อและบริการของเราติดต่อ 0926516944 , 02 4243434, 02 434 3434
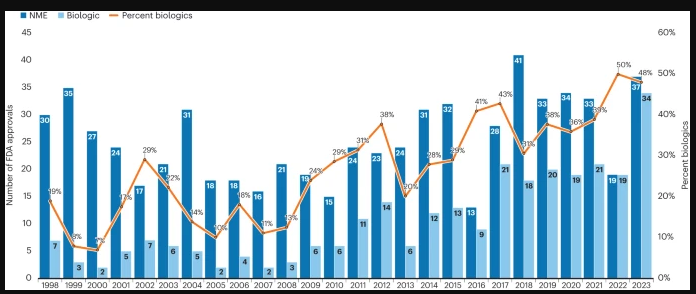
ปี 2023 FDA อนุมัติยามากที่สุดเป็นประวัติการณ์

FDA สร้างสถิติใหม่ อนุมัติยาทั้งหมด 71 รายการ ในปี 2023 โดยรวมถึงการบําบัดรักษาด้วยยีนถึง 5 รายการ ในจํานวนนี้ เป็นเทคโนโลยี CRISPR-Cas9 ส่วน Leqembi ยารักษาโรคอัลไซเมอร์ก็ผ่านความเห็นชอบให้วางจําหน่ายใน สหรัฐอเมริกาเช่นกัน
ในช่วงที่เกิดวิกฤตโควิด-19 ทั่วโลกโดยเฉพาะในปี 2022 สํานักงานคณะกรรมการอาหารและยาแห่งสหรัฐอเมริกา (FDA) อนุมัติยาใหม่เพียง 37 รายการ ซึ่งถือว่าตํ่าสุดในรอบ 6 ปี โดย 41% ของยาที่ผ่านการอนุมัติเป็นยาชีวภาพ แต่ FDA กลับมาทํางานตรวจสอบยาใหม่อย่างเข้มข้นขึ้นอีกภายหลัง การสิ้นสุดภาวะฉุกเฉินด้านสาธารณสุขจากโรคโควิด-19 ในสหรัฐอเมริกาอย่างเป็นทางการในเดือนพฤษภาคม ปี 2023 โดยมีรายการยาใหม่เพียง 1 หรือ 2 รายการเท่านั้นที่เป็นข้อ
ขัดแย้งในคณะกรรมการพิจารณายา และไม่ได้ผ่านการอนุมัติในระดับเฟิร์สคลาส แต่โดยรวมแล้ว FDA อนุมัติยาใหม่มากที่สุดเป็นประวัติการณ์ ทําลายสถิติเดิมอย่างสิ้นเชิง จากที่เคยอนุมัติยาใหม่สูงที่สุด 59 รายการ ในปี 2018 แตล่าสุดในปี 2023 เพิ่มเป็น 71 รายการ โดย 48% ของยาใหม่ทั้งหมดเป็นยาชีวภาพ สะท้อนให้เห็นถึงความก้าวหน้าอย่างต่อเนื่องของการรักษาทางชีวภาพรูปแบบใหม่ ๆ
หนึ่งในรายการอนุมัติที่เป็นเทคโนโลยีดานการบําบัดโรค ด้วยการตัดต่อทางพันธุกรรม หรือ CRISPR–Cas9 ที่ FDA อนุมัติเป็นครั้งแรก คือ exagamglogene autotemcel หรือ ชื่อทางการค้าว่า Casgevy ของบริษัท Vertex Pharmaceuticals และ CRISPR Therapeutics สําหรับการรักษาธาลัสซีเมีย แบบบีตา และโรคเม็ดเลือดแดงรูปเคียว (Sickle Cell Disease - SCD) ในผู้ป่วย อายุ 12 ปีขึ้นไป ที่มักมีอาการวิกฤตหลอดเลือดอุดตัน (VOCs) นับเป็น
ครั้งแรกที่ผู้ป่วย SCD ประมาณ 16,000 ราย ในสหรัฐฯ จะมีสิทธิ์ได้รับการรักษาด้วยเทคโนโลยี CRISPR–Cas9 โดยก่อนหน้านี้สหราชอาณาจักร และซาอุดีอาระเบียได้อนุมัติ Casgevy ในการรักษา 2 โรคดังกล่าวไปแล้ว ส่วนสหภาพยุโรปกําลังอยู่ในขั้นตอนพิจารณาอนุมัติ นอกจากนี้ FDA
ยังอนุมัติการจําหน่ายยาชีวภาพ ที่ชื่อ Lyfgenia (lovotibeglogeneautotemcel) ของบริษัท Bluebird bio ที่ใช้รักษา SCD เช่นกันซึ่ง Lyfgenia จะช่วยเพิ่มยีน β-globin เพื่อผลิต HbAT87Q ทดแทนฮีโมโกลบินที่เสียหาย
ส่วนยารักษาโรคอัลไซเมอร์ ที่มีชื่อว่า Lecanemab (หรือชื่อทางการค้าว่า Leqembi) เพิ่งได้รับการอนุมัติให้วางจําหน่ายในสหรัฐฯ ได้ หลังจากญี่ปุนและจีนอนุมัติยาตัวนี้ไปก่อนหน้านี้แล้ว ขณะที่ยุโรปกําลังอยู่ระหว่างการพิจารณา สําหรับยา Leqembi ซึ่งผลิตโดยบริษัท Eisai และ Biogen Leqembi เป็นแอนติบอดีที่ออกแบบมาเพื่อขจัดก้อนโปรตีนผิดปกติที่เรียกว่า อะไมลอยด์เบต้า (Aβ or Abeta) ออกจากสมองของผู้ป่วยอัลไซเมอร์ การรักษาด้วยยาชีวภาพนี้ใช้ได้ผลดีในระยะแรกของโรคเพื่อชะลอการลุกลามของโรคอัลไซเมอร์
นอกจากนี้ ศูนย์ประเมินและวิจัยยาของเอฟดีเอ (CDER) อนุมัติ การบําบัดด้วยเอนไซม์ทดแทน (ERT) เป็นครั้งแรก นั่นคือ ADZYNMA (ADAMTS13, recombinant-krhn) ของบริษัท Takeda อันเป็นการบําบัดแบบเวชศาสตร์ป้องกันสําหรับ congenital thrombotic thrombocytopenic purpura (cTTP) ในผู้ป่วยผู้ใหญ่และเด็ก CDER ยังได้เห็นชอบกับแคปซูลยาไมโครไบโอมที่เรียกว่า Vowst จากบริษัท Seres Therapeutics อันเป็นการรักษาด้วยแบคทีเรียที่ได้จากมนุษย์เพื่อป้องกันการติดเชื้อ Clostridioides diffi cile (C. diff) ในผู้ป่วยที่มีอายุ 18 ปีขึ้นไป
กว่าครึ่งหนึ่งของยาที่ FDA อนุมัติในปี 2023 เป็นยากําพร้า สําหรับโรคหายาก ส่วนยาประเภทที่ผลิตจากแอนติบอดีและ smalll molecules อย่่าง RNA มีแนวโน้มว่าจะออกสู่ตลาด มากขึ้น และจะมีมูลค่ามากกว่า 6 หมื่นล้านดอลลาร์สหรัฐ ภายใน 4 ปีข้างหน้า หลังจากในปี 2023 FDA อนุมัติยาใหม่ 4 รายการที่ใช้ oligonucleotide เป็นหลัก Abrysvo ของ Pfi zer และ Arexvy ของ GSK ซึ่งเป็นวัคซีนป้องกันไวรัส RSV ทั้งคู่ก็ได้รับการอนุมัติเป็นครั้งแรกเมื่อปีที่แล้ว ซึ่งมีประสิทธิภาพในการระงับ การแพร่กระจายของไวรัส RSV ในระบบทางเดินหายใจทั้งส่วนบนและส่วนล่างของทารกหลังคลอดใหม่ ๆ ส่วนยาแอนติบอดีป้องกัน RSV อย่าง Beyfortus (nirsevimab) ของบริษัท Sanofi กับ AstraZeneca ผ่านการอนุมัติจาก FDA เช่นกัน โดยใช้ฉีดทารกที่มีความเสี่ยงสูงเพียงครั้งเดียว ไม่เหมือน Synagis (palivizumab) ของบริษัท Sobi ที่ต้องฉีดให้ทารกอายุตํ่ากว่า 2 ขวบ เดือนละครั้ง ติดต่อกัน 5 เดือน
ส่วนยาลดนํ้าหนักสําหรับผู้ที่เป็นโรคอ้วนอย่าง Zepbound (tirzepatide) ที่ใช้เป็นยารักษาโรคเบาหวานของบริษัท Eli Lilly หลังจากผ่านการอนุมัติจาก FDA คาดว่ายอดขายจะแซงหน้ายา Wegovy (semaglutide) ของ Novo Nordisk ขณะที่ปัจจุบัน ตลาดยาลดนํ้าหนักมีมูลค่าสูงกว่า 1 แสนล้านดอลลาร์สหรัฐ ขณะที่ตลาดยา Antibody-drug conjugates (ADCs) ที่ใช้รักษาโรคมะเร็งชนิดต่าง ๆ ก็ขยายตัว 11.2% จากปี 2022 ที่มีมูลค่าเกือบ 8 พันล้านดอลลาร์สหรัฐ โดยภายปีนี้คาดว่าจะสูงถึง 1 หมื่น 2 พันล้านดอลลาร์สหรัฐ
ส่วนรายการยาและการบําบัดสําคัญที่คาดว่าจะผ่านการ อนุมัติจาก FDA ภายในปี 2024 นี้ ได้แก่ thyroid hormone receptor-β selective agonist resmetirom ของ Madrigal Pharmaceuticals สําหรับโรคไขมันพอกตับที่ไม่ได้เกิดจากการดื่มแอลกอฮอล์และการเกิดพังผืดในตับ Tarlatamab ของ Amgen สําหรับการรักษามะเร็งเซลล์ขนาดเล็กของปอด Zanidatamab ของ Jazz Pharmaceuticals ซึ่งเป็นโปรตีนฟิวชันที่ออกฤทธิ์ในภาวะความดันโลหิตสูง ในหลอดเลือดแดงของปอด Crovalimab ของ Roche และ Chugai Pharmaceutical สําหรับการบําบัดโรค paroxysmal nocturnal hemoglobinuria (PNH) รวมทั้ง Eculizumab ที่เป็น recombinantmonoclonal antibody สําหรับการบําบัด PNH เช่นกัน ขณะนี้อยู ระหว่างการศึกษาทางคลินิกของบริษัท Amgen และ Daiichi

