สนใจทำการตลาดผ่านสื่อและบริการของเราติดต่อ 063-932-1441 , 02 4243434, 02 434 3434
ข้อมูลสำคัญของ Sotagliflozin ในผู้ป่วยเบาหวานที่มีโรคไตเรื้อรังร่วมด้วย
ผลวิเคราะห์เป้าประสงค์รองของ SCORED randomized trial พบว่า dual SGLT1/2 inhibitor sotagliflozinลดความเสี่ยงของการเกิด MACE ลงได้อย่างมีนัยสำคัญในผู้ป่วยเบาหวานชนิดที่ 2 ที่มีโรคไตเรื้อรังร่วมด้วย โดย sotagliflozinถือเป็น SGLT inhibitor ตัวแรกที่สามารถลดความเสี่ยงของการเกิด MI และ stroke ลงได้อย่างมีนัยสำคัญ
ผลการวิเคราะห์เป้าประสงค์รองที่กำหนดไว้ตั้งแต่ต้น (prespecified secondary analysis) ของการศึกษาทางคลินิกขนาดใหญ่ที่มีชื่อว่า SCORED ซึ่งดำเนินการโดยนายแพทย์ Rahul Aggarwal (Brigham and Women's Hospital Heart and Vascular Center, Harvard Medical School, Boston, Massachusetts, USA) และคณะ พบว่า sotagliflozin (ขนาด 200 mg รับประทานเพียงวันละครั้งและสามารถเพิ่มขนาดเป็น 400 mg รับประทานเพียงวันละครั้งในช่วง 6 เดือนแรก หากไม่มีผลข้างเคียงที่รุนแรงใดๆ เกิดขึ้น) สามารถลดความเสี่ยงของการเกิด major adverse cardiovascular events หรือ MACE (composite of cardiovascular death, non-fatal MI, and non-fatal stroke) ลงได้ถึง 23% ในผู้ป่วยที่จัดว่าเป็นกลุ่มที่มีความเสี่ยงสูง เนื่องจากป่วยเป็นเบาหวานชนิดที่ 2 ที่มีโรคไตเรื้อรังร่วมด้วยและมีปัจจัยเสี่ยงของโรคระบบหัวใจและหลอดเลือดอยู่ด้วยเช่น นอนโรงพยาบาล เนื่องจากมีภาวะหัวใจล้มเหลวในช่วง 2 ปีก่อนเข้าร่วมการศึกษามีค่าความสามารถในการบีบตัวของหัวใจ (ejection fraction, EF) เท่ากับหรือน้อยกว่า 40% หรือมีภาวะหัวใจห้องล่างซ้ายหนาตัว (left ventricular hypertrophy) โดยเฉพาะอย่างยิ่งพบว่า sotagliflozin สามารถลดความเสี่ยงของการเกิดภาวะกล้ามเนื้อหัวใจขาดเลือด (myocardial infarction, MI) ลงได้ถึง 32% และโรคหลอดเลือดสมอง (stroke) ลงได้ถึง 34%
ผลวิเคราะห์ที่น่าสนใจดังกล่าวของ sotagliflozin ได้รับการเผยแพร่ผ่านทางเว็บไซต์ของวารสารการแพทย์ Lancet Diabetes & Endocrinology เมื่อวันที่ 14 กุมภาพันธ์ 2568
ขณะที่ SCORED เป็นการศึกษาทางคลินิกแบบ double-blind, placebo-controlled, randomized clinical trial ในผู้ป่วยเบาหวานชนิดที่ 2 อายุตั้งแต่ 18 ปีขึ้นไป จำนวนทั้งสิ้น 10,584 คน ที่มีโรคไตเรื้อรังร่วมด้วย (มี estimated glomerular filtration rate หรือ eGFR 25–60 mL/min per 1·73 m2) และปัจจัยเสี่ยงของโรคระบบหัวใจและหลอดเลือดอยู่ด้วย โดยเกือบ 50% ของผู้ป่วยเหล่านี้มีประวัติของโรคระบบหัวใจและหลอดเลือด (cardiovascular disease), 19.9% มีประวัติของ MI, 8.9% มีประวัติของโรคหลอดเลือดสมอง และ 22.4% ผ่านการทำ coronary revascularization ผู้ป่วยเหล่านี้ถูกสุ่ม (1:1) ออกเป็น 2 กลุ่ม กลุ่มหนึ่งจำนวน 5,292 คน ได้รับ sotagliflozin ขณะที่อีกกลุ่มหนึ่งจำนวน 5,292 คนเช่นกัน ได้รับ matching placebo โดยมี MACE เป็น prespecified secondary outcome
จากการติดตามผู้ป่วยเป็นเวลาโดยเฉลี่ย 14.2 เดือน พบว่ากลุ่มผู้ป่วยที่ได้รับ sotagliflozin มีอัตราของ MACE อยู่ที่ 4.8 events per 100 person-years เทียบกับ 6.3 events per 100 person-years ของกลุ่มผู้ป่วยที่ได้รับ placebo [hazard ratio (HR) 0.77, 95% confidence interval (CI) 0.65-0.91, P=0.0020)โดยมีอัตราของ MI event อยู่ที่ 1.8 เทียบกับ 2.7 per 100 person-years ของกลุ่มผู้ป่วยที่ได้รับ placebo (HR 0.68, 95% CI 0.52-0.89, P=0.0041) และ stroke event อยู่ที่ 1.2 เทียบกับ 1.8 events per 100 person-years (HR 0.66, 95% CI 0.48-0.91, P=0.012)
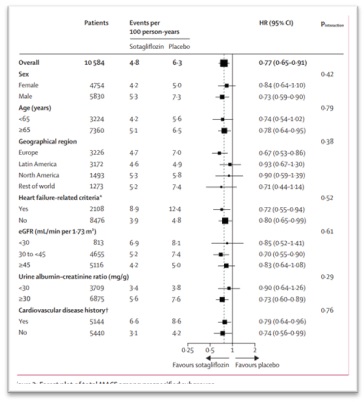
นายแพทย์ Rahul Aggarwal และคณะระบุว่า sotagliflozin เป็นยาตัวแรกในกลุ่ม sodium-glucose cotransporter inhibitor หรือ SGLT inhibitor ที่มีหลักฐานแสดงให้เห็นว่าสามารถลดความเสี่ยงของการเกิดภาวะกล้ามเนื้อหัวใจขาดเลือดและโรคหลอดเลือดสมองได้อย่างมีนัยสำคัญ ซึ่งเป็นผลจากการที่ sotagliflozin มีกลไกการออกฤทธิ์ที่เป็นเอกลักษณ์เฉพาะตัวนั่นก็คือ นอกจากจะยับยั้งตัวรับของ sodium-glucose cotransporter type 2 (SGLT2 receptors) ที่พบได้ในไตแล้ว ยังยับยั้งตัวรับของ sodium-glucose cotransporter type 1 (SGLT1 receptors) ที่พบได้ในไต ลำไส้ หัวใจและสมอง ควบคู่กันไปด้วย
อนึ่ง ในเดือนพฤษภาคม 2566 สำนักงานอาหารและยาของสหรัฐอเมริกา (Food and Drug Administration หรือ FDA) ให้การรับรอง sotagliflozin (Inpefa) ด้วยข้อบ่งใช้สำหรับลดความเสี่ยงของ cardiovascular death, hospitalization for heart failure และ urgent heart failure visitในผู้ป่วยภาวะหัวใจล้มเหลวอายุตั้งแต่ 18 ปีขึ้นไป (ทั้ง heart failure with preserved ejection fraction หรือ HFpEFและ heart failure with reduced ejection fraction หรือ HFrEF) และด้วยข้อบ่งใช้สำหรับลดความเสี่ยงของ cardiovascular death, hospitalization for heart failure และ urgent heart failure visit ในผู้ป่วยเบาหวานชนิดที่ 2, ผู้ป่วยโรคไตเรื้อรังและผู้ป่วยที่มี cardiovascular risk factors อื่นๆ ด้วย
ข้อมูลสำคัญที่ FDA ใช้ประกอบการพิจารณาให้การรับรอง sotagliflozin ในข้อบ่งใช้ดังกล่าวก็คือผลลัพธ์ของ 2 การศึกษาทางคลินิกแบบ randomized, double-blind, placebo-controlled Phase 3 cardiovascular outcomes studies ได้แก่ SCORED และ SOLOIST-WHF โดยผลการศึกษาของ SCORED (Sotagliflozin in Patients with Diabetes and Chronic Kidney Disease) ที่รายงานไว้ในวารสารการแพทย์ New England Journal of Medicine (NEJM) ฉบับวันที่ 16 พฤศจิกายน 2563 พบว่า sotagliflozin สามารถลดความเสี่ยงของ composite of deaths from cardiovascular causes, hospitalizations for heart failure และ urgent visits for heart failure ได้ดีกว่า placebo ในผู้ป่วยเบาหวานชนิดที่ 2 อายุตั้งแต่ 18 ปีขึ้นไปที่มีโรคไตเรื้อรังร่วมด้วย
ขณะที่ผลการศึกษาของ SOLOIST-WHF (Sotagliflozin in Patients with Diabetes and Recent Worsening Heart Failure) ที่รายงานไว้ในวารสารการแพทย์ NEJM ฉบับวันที่ 16 พฤศจิกายน 2563 เช่นกัน พบว่าการเริ่มให้ยา sotagliflozin ก่อน discharge หรือภายในเวลาไม่นานหลังจาก discharge ในผู้ป่วยเบาหวานชนิดที่ 2 ที่เพิ่งจะเข้านอนโรงพยาบาลเนื่องจากมีภาวะหัวใจล้มเหลวที่แย่ลง สามารถลดความเสี่ยงของ deaths from cardiovascular causes, HF hospitalizations และ urgent visits for heart failure ได้ดีกว่าอย่างมีนัยสำคัญเมื่อเทียบกับ placebo
แหล่งที่มาของข้อมูล: www.medpagetoday.com, www.thelancet.com, www.drugs.com, www.cardiometabolichealth.org, www.mountsinai.org, www.nejm.org

