สนใจทำการตลาดผ่านสื่อและบริการของเราติดต่อ 0926516944 , 02 4243434, 02 434 3434
US FDA อนุมัติใช้ยาฉีด Ozempic (semaglutide) ยาตัวแรกในกลุ่ม GLP-1 RAsสำหรับผู้ป่วยT2DM & CKD

Ozempic (semaglutide)กลายเป็นยาฉีดในกลุ่ม GLP-1 RAs ตัวแรกและตัวเดียวเท่านั้นในปัจจุบันที่มีข้อบ่งใช้จากการรับรองของสำนักงานอาหารและยาของสหรัฐอเมริกาสำหรับลดความเสี่ยงของโรคไตที่แย่ลง ไตวายและการเสียชีวิตจากโรคระบบหัวใจและหลอดเลือดในผู้ป่วยเบาหวานชนิดที่ 2 ที่มีโรคไตเรื้อรังร่วมด้วย
เมื่อวันที่ 28 มกราคม 2568 Novo Nordisk แจ้งว่าสำนักงานอาหารและยาของสหรัฐอเมริกา (Food and Drug Administration หรือ FDA) ให้การรับรอง Ozempic (semaglutide) เพื่อใช้สำหรับลดความเสี่ยงของโรคไตที่แย่ลง (kidney disease worsening), ไตวาย (end-stage kidney disease) และการเสียชีวิตจากโรคระบบหัวใจและหลอดเลือด(death due to cardiovascular disease) ในผู้ป่วยโรคเบาหวานชนิดที่ 2 (type 2 diabetes mellitus หรือ T2DM) อายุตั้งแต่ 18 ปีขึ้นไปที่มีโรคไตเรื้อรัง (chronic kidney disease หรือ CKD) ร่วมด้วย
ด้วยข้อบ่งใช้ล่าสุดดังกล่าวที่ได้รับการรับรองจาก FDA นอกจากจะทำให้ Ozempic (semaglutide) ซึ่งบริหารยาด้วยการฉีดเข้าชั้นใต้ผิวหนัง (subcutaneous injection) เพียงสัปดาห์ละครั้ง กลายเป็นยาฉีดในกลุ่ม glucagon-like peptide-1 receptor agonists (GLP-1 RAs) ตัวแรกและตัวเดียวเท่านั้นในปัจจุบันที่แพทย์สามารถสั่งจ่ายให้กับผู้ป่วยเพื่อลดความเสี่ยงของโรคไตที่แย่ลง ไตวายและการเสียชีวิตจากโรคระบบหัวใจและหลอดเลือดในผู้ป่วยเบาหวานชนิดที่ 2 อายุตั้งแต่ 18 ปีขึ้นไปที่มีโรคไตเรื้อรังร่วมด้วยแล้ว ยังมีผลให้ Ozempic (semaglutide) เป็น GLP-1 RA ที่มีข้อบ่งใช้ครอบคลุมกว้างขวางมากที่สุด คือใช้ร่วมกับการควบคุมอาหารและการออกกำลังกายเพื่อเพิ่มประสิทธิภาพในการควบคุมระดับน้ำตาลในเลือดในผู้ป่วยเบาหวานชนิดที่ 2 อายุตั้งแต่ 18 ปีขึ้นไปและใช้เพื่อลดความเสี่ยงของ major cardiovascular events เช่น ภาวะกล้ามเนื้อหัวใจขาดเลือดเฉียบพลัน โรคหลอดเลือดสมองและการเสียชีวิต ในผู้ป่วยเบาหวานชนิดที่ 2 อายุตั้งแต่ 18 ปีขึ้นไปที่มีโรคหัวใจอยู่แล้ว
สำหรับข้อมูลสำคัญที่ FDA ใช้ประกอบการพิจารณาให้การรับรอง Ozempic (semaglutide) ในข้อบ่งใช้ล่าสุดดังกล่าวก็คือ ผลการศึกษาของการศึกษาทางคลินิกขนาดใหญ่ที่มีชื่อว่า FLOW (Effects of Semaglutide on Chronic Kidney Disease in Patients with Type 2 Diabetes) ซึ่งเป็นการศึกษาแบบ randomized, double-blind, parallel-group, event-driven, phase 3b superiority trial ในผู้ป่วยเบาหวานชนิดที่ 2 อายุตั้งแต่ 18 ปีขึ้นไปและมีโรคไตเรื้อรังร่วมด้วย (มีค่า estimated glomerular filtration rate หรือ eGFR ตั้งแต่ 50 ไปจนถึง 70 ml/minute/1.73 m2 และมี urinary albumin-to-creatinine ratioหรือ UACR มากกว่า 300 ไปจนถึงน้อยกว่า 5,000 mg/g หรือมีค่า eGFR เท่ากับหรือมากกว่า 25 ไปจนถึงน้อยกว่า 50 ml/min/1.73 m2 และ UACR มากกว่า 100 ไปจนถึงน้อยกว่า 5,000 mg/g) จำนวนทั้งสิ้น 3,533 คน โดยผู้ป่วยถูกสุ่ม (1:1) ออกเป็น 2 กลุ่ม กลุ่มหนึ่งจำนวน 1,767 คนได้รับ Ozempic (semaglutide) 1.0 mg ฉีดเข้าชั้นใต้ผิวหนังเพียงสัปดาห์ละครั้ง ขณะที่อีกกลุ่มหนึ่งจำนวน 1,766 คนได้รับ matching placeboเสริมเข้ากับการรักษาที่เป็น standard of care คือrenin-angiotensin-aldosterone system (RAAS) blockade เช่น ยากลุ่ม angiotensin-converting enzyme inhibitors (ACEIs) และยากลุ่ม angiotensin II receptor antagonists (ARBs)
FLOW มีเป้าประสงค์หลักที่เป็น kidney outcomes อยู่ที่การลดอุบัติการณ์ของ primary composite endpoint ซึ่งประกอบด้วย time to first occurrence of: ≥50% sustained eGFR decline, kidney failure (sustained eGFR 2, initiation of long-term dialysis, or transplantation) และ/หรือ renal death or CV deathโดยเมื่อเริ่มต้นการศึกษา ผู้ป่วยเบาหวานชนิดที่ 2 ที่ร่วมอยู่ในการศึกษามี mean eGFR อยู่ที่ 47 mL/min/1.73 m2และ median UACR อยู่ที่ 568 mg/g (11% ของผู้ป่วยมี eGFR 2 และ 69% มี UACR >300 mg/g เมื่อเริ่มต้นการศึกษา)
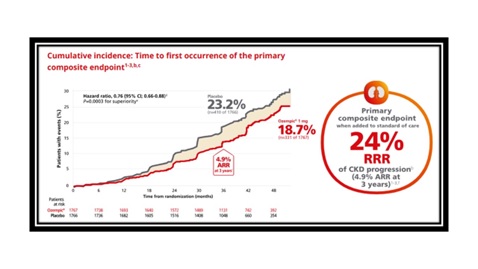
ผลการศึกษาของ FLOW ที่ได้รับการตีพิมพ์ในวารสารการแพทย์ New England Journal of Medicine(NEJM)ฉบับประจำวันที่ 24 พฤษภาคม 2567 จากการติดตามผู้เข้าร่วมการศึกษาเป็นเวลาเฉลี่ย 3.4 ปีและการศึกษานี้ถูกยุติลงก่อนกำหนดตามคำแนะนำของ Independent Data Monitoring Committee พบว่า Ozempic (semaglutide) มีประสิทธิภาพเหนือกว่า placebo อย่างมีนัยสำคัญในการลดความเสี่ยงของ kidney disease worsening, kidney failure และ death due to cardiovascular disease โดยมีrelative risk reductionอยู่ที่ 24% และ 4.9% absolute risk reduction ที่ 3 ปี
ขณะเดียวกันพบว่า Ozempic (semaglutide) ขนาด 1.0 mg ฉีดเข้าชั้นใต้ผิวหนังเพียงสัปดาห์ละครั้ง มีประสิทธิภาพเหนือกว่า placebo ในทุก confirmatory secondary outcomes ได้แก่ การลดลงอย่างมีนัยสำคัญของ mean annual eGFR) slope อยู่ที่ 1.16 ml/min/1.73 m²/year (-2.19 เทียบกับ -3.36 ml/min/1.73 m²/year [0.86; 1.47]; P<0.001), ความเสี่ยงที่ลดลงของการเกิด major cardiovascular events(212 เทียบกับ 254 events; hazard ratio: 0.82; [0.68; 0.98]; P=0.029) และความเสี่ยงที่ลดลงของ death from any cause (227 เทียบกับ 279 events; hazard ratio: 0.80 [0.67; 0.95]; P=0.01)
ส่วนข้อมูลด้านความปลอดภัยของ FLOW พบว่ามีรายงานของอุบัติการณ์ไม่พึงประสงค์ที่รุนแรง(serious adverse events) เกิดขึ้นใน 877 ราย (49.6%) ของกลุ่มที่ได้รับ Ozempic (semaglutide) ขนาด 1.0 mg ฉีดเข้าใต้ชั้นผิวหนังเพียงสัปดาห์ละครั้ง เทียบกับใน 950 คน (53.8%) ของกลุ่มที่ได้รับ placebo สำหรับ adverse events หลักที่ทำให้ต้องหยุดยาอย่างถาวรที่มีรายงานพบได้บ่อยมากกว่าในกลุ่มที่ได้รับ Ozempic (semaglutide) เมื่อเทียบกับกลุ่มที่ได้รับ placebo คือ gastrointestinal disorders [79 (4.5%) เทียบกับ 20 คน (1.1%)]
อนึ่ง Ozempic (semaglutide) ขนาด 0.5 mg และ 1.0 mg ฉีดเข้าชั้นใต้ผิวหนังเพียงสัปดาห์ละครั้ง ได้รับการรับรองจาก FDA เป็นครั้งแรกในเดือนธันวาคม 2560 ด้วยข้อบ่งใช้สำหรับเสริมเข้ากับการควบคุมอาหารและการออกกำลังกายเพิ่มประสิทธิภาพในการควบคุมระดับน้ำตาลในเลือดในผู้ป่วยเบาหวานชนิดที่ 2 อายุตั้งแต่ 18 ปีขึ้นไป โดยผลวิเคราะห์จาก global SUSTAIN clinical trial programmeที่ประกอบด้วยphase 3a trials 8 การศึกษาในผู้ป่วยเบาหวานชนิดที่ 2 อายุตั้งแต่ 18 ปีขึ้นไป จำนวนรวมกันกว่า 8,000 คน พบว่า Ozempic (semaglutide)ฉีดเข้าชั้นใต้ผิวหนังเพียงสัปดาห์ละครั้งร่วมกับการควบคุมอาหารและการออกกำลังกาย สามารถลดระดับน้ำตาลสะสมในเลือดในช่วง 3 เดือนที่ผ่านมา ได้ดีกว่าอย่างมีนัยสำคัญทางสถิติเมื่อเทียบกับ placebo
นอกจากนี้ ในเดือนมกราคม 2563 FDA ได้ให้การรับรองข้อบ่งใช้ใหม่เพิ่มเติมของ Ozempic (semaglutide) ขนาด 0.5 mg หรือ 1.0 mg ฉีดเข้าชั้นใต้ผิวหนังเพียงสัปดาห์ละครั้ง นั่นก็คือใช้เพื่อลดความเสี่ยงของการเกิด major adverse cardiovascular events หรือ MACE เช่น ภาวะกล้ามเนื้อหัวใจขาดเลือดเฉียบพลัน โรคหลอดเลือดสมองและการเสียชีวิตจากโรคระบบหัวใจและหลอดเลือดในผู้ป่วยเบาหวานชนิดที่ 2 อายุตั้งแต่ 18 ปีขึ้นไปที่เป็นโรคหัวใจอยู่แล้ว
แหล่งที่มาของข้อมูล: www.drugs.com,www.kidney.org, www.webmd.com, www.novonordisk-us.com,www.nejm.org, www.multivu.com, www.prnewswire.com

