ผู้ที่มีภาวะน้ำหนักเกินหรือเป็นโรคอ้วนในสหรัฐอเมริกา มีทางเลือกสำหรับใช้ในการรักษาเพิ่มขึ้นหลังจากสำนักงานอาหารและยาของสหรัฐอเมริกาให้การรับรอง tirzepatide ด้วยข้อบ่งใช้ฉีดเข้าทางผิวหนังเพียงสัปดาห์ละครั้ง เสริมเข้ากับการควบคุมการรับประทานอาหารที่ให้พลังงานสูงและการเพิ่มกิจกรรมทางกาย โดยเฉพาะการออกกำลังกายอย่างสม่ำเสมออยู่เป็นประจำทุกวัน
เมื่อวันพุธที่ 8 พฤศจิกายน 2566 สำนักงานอาหารและยาของสหรัฐอเมริกา (Food and Drug Administration หรือ FDA) ให้การรับรอง tirzepatide หรือที่มีชื่อทางการค้าว่า Zepbound สำหรับใช้เป็น chronic weight management เสริมเข้ากับ reduced calorie diet และ increased physical activity ในผู้ที่มีอายุตั้งแต่ 18 ปีขึ้นไป ที่มีภาวะน้ำหนักเกิน (overweight คือ มีดัชนีมวลกาย หรือ body mass index หรือ BMI ตั้งแต่ 27 kg/m2 ขึ้นไป) หรือเป็นโรคอ้วน obesity คือ มีดัชนีมวลกาย หรือ BMI เท่ากับหรือมากกว่า 30 kg/m2 ขึ้นไป และมี weight-related condition ร่วมด้วยอย่างน้อย 1 อย่าง เช่น ความดันโลหิตสูง เบาหวาน ชนิดที่ 2 หรือภาวะไขมันคอเลสเตอรอลในเลือดสูง โดย tirzepatide (Zepbound) injection 0.5 mL บริหารยาด้วยการฉีดเข้าชั้นใต้ผิวหนัง (subcutaneous injection) เพียงสัปดาห์ละครั้ง โดยขนาดเริ่มต้นที่แนะนำ คือ 2.5 mg เพียงสัปดาห์ละครั้ง และสามารถปรับเพิ่มขนาดยาเป็น 5 mg เพียงสัปดาห์ละครั้ง หลังจาก 4 สัปดาห์ ส่วน maintenance doses ที่แนะนำ คือ 5 mg, 10 mg หรือ 15 mg ซึ่ง available strengths ของ tirzepatide (Zepbound) จะมีตั้งแต่ 2.5 mg/0.5 mL, 5 mg/0.5 mL, 7.5 mg/0.5 mL, 10 mg/0.5 mL, 12.5 mg/0.5 mL ไปจนถึง 15 mg/0.5 mL
นพ. John Sharretts ผู้อำนวยการแผนก Diabetes, Lipid Disorders และ Obesity แห่งศูนย์วิจัยและประเมินยา (Center for Drug Evaluation and Research) ของ FDA กล่าวว่า โรคอ้วนและภาวะน้ำหนักเกินเป็น serious conditions ที่มีความสัมพันธ์กับโรคที่เป็นสาเหตุอันดับต้น ๆ ของการเสียชีวิต เช่น โรคหัวใจ โรคหลอดเลือดสมอง และโรคเบาหวาน ดังนั้น การที่ FDA ให้การรับรอง tirzepatide (Zepbound) ซึ่งเป็นห้วงเวลาที่กำลังมีอัตราการเพิ่มขึ้นอย่างรวดเร็วของทั้งผู้ที่เป็นโรคอ้วนและผู้ที่มีภาวะน้ำหนักเกินในสหรัฐอเมริกา จึงเท่ากับเป็นการตอบสนองต่อ unmet medical need ในเรื่องนี้ โดยจากข้อมูลของศูนย์ควบคุมและป้องกันโรคของสหรัฐอเมริกา (Centers for Disease Control and Prevention หรือ CDC) พบว่า ปัจจุบันถึงราว ๆ 70% ของชาวอเมริกันที่อยู่ในวัยผู้ใหญ่ มีภาวะน้ำหนักเกินหรือเป็นโรคอ้วน และผู้ที่มีภาวะน้ำหนักเกินจำนวนมากต่างก็มี weight-related condition มากกว่า 1 อย่าง
Tirzepatide ซึ่งเป็น active ingredient ของ Zepbound ถือเป็นยาตัวแรกของยากลุ่มใหม่ที่มีกลไกการออกฤทธิ์เป็น dual GLP-1/ GLP-1 receptor agonist กล่าวคือ ออกฤทธิ์กระตุ้น receptors ของทั้ง glucagon-like peptide-1 หรือ GLP-1 และ glucose-dependent insulinotropic polypeptide (GIP) ไปพร้อม ๆ กัน จึงสามารถลดน้ำตาลในเลือดและลดความอยากอาหาร (appetite) ได้เป็นอย่างดี โดยก่อนหน้านี้ในเดือนพฤษภาคม 2565 tirzepatide หรือที่มีชื่อทางการค้าว่า Mounjaro ได้รับการรับรองจาก FDA ในข้อบ่งใช้สำหรับการช่วยเพิ่มประสิทธิภาพในการควบคุมระดับน้ำตาลในเลือดด้วยการเสริมเข้ากับ reduced calorie diet และ increased physical activity ในผู้ป่วยเบาหวาน ชนิดที่ 2 ที่มีอายุตั้งแต่ 18 ปีขึ้นไป
สำหรับข้อมูลด้านประสิทธิภาพและความปลอดภัยของ tirzepatide (Zepbound) ที่นำมาสู่การได้รับการรับรองจาก FDA ในข้อบ่งใช้สำหรับ chronic weight management นั้น มาจาก 2 การศึกษาทางคลินิกขนาดใหญ่แบบ phase 3 double-blind, randomized, controlled trial ที่มีชื่อว่า SURMOUNT-1 และ SURMOUNT-2 โดย SURMOUNT-1 ทำในผู้ที่มีอายุตั้งแต่ 18 ปีขึ้นไป ที่มีภาวะน้ำหนักเกิน หรือเป็นโรคอ้วนที่มี weight-related condition ร่วมด้วยอย่างน้อย 1 อย่าง ยกเว้นเบาหวาน จำนวน 2,539 คน ซึ่งถูกสุ่มแบ่งออกเป็น 4 กลุ่ม เปรียบเทียบระหว่างการได้รับ tirzepatide (Zepbound) 5 mg, 10 mg และ 15 mg ฉีดเข้าชั้นใต้ผิวหนังเพียงสัปดาห์ละครั้ง และการได้รับ placebo เป็นเวลา 72 สัปดาห์ สำหรับ coprimary endpoints ของการศึกษานี้ คือ % การเปลี่ยนแปลงของน้ำหนักตัวที่ 72 สัปดาห์ จากเมื่อเริ่มต้นการศึกษา (baseline) และจำนวนผู้ที่สามารถลดน้ำหนักตัวลงได้ตั้งแต่ 5% ขึ้นไป โดยเมื่อเริ่มต้นการศึกษา ผู้เข้าร่วมการศึกษาส่วนใหญ่มี mean body weight อยู่ที่ 104.8 kg มี mean BMI was 38.0 และ 94.5% ของผู้เข้าร่วมการศึกษามี BMI เท่ากับ 30 หรือสูงกว่า 30 ขึ้นไป ซึ่งเท่ากับว่าผู้เข้าร่วมในการศึกษานี้ส่วนใหญ่เป็นโรคอ้วน
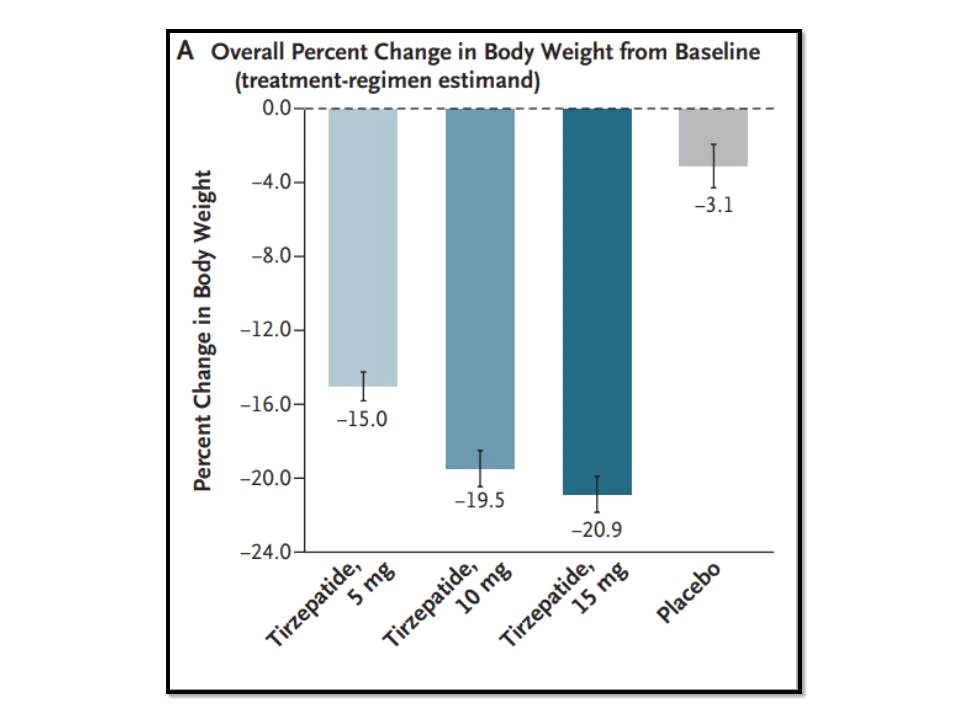
ผลการศึกษาของ SURMOUNT-1 ที่รายงานไว้ใน New England Journal of Medicine (NEJM) ฉบับประจำวันที่ 21 กรกฎาคม 2565 พบว่า มี mean percentage change ของน้ำหนักตัวที่ 72 สัปดาห์ จากเมื่อเริ่มต้นการศึกษา อยู่ที่ -15.0%, -19.5% และ -20.9% สำหรับกลุ่มที่ได้รับ tirzepatide (Zepbound) 5 mg, 10 mg และ 15 mg ตามลำดับ เทียบกับ -3.1% ของกลุ่มที่ได้รับ placebo ซึ่งแตกต่างกันอย่างมีนัยสำคัญทางสถิติ ขณะเดียวกันพบว่ามี % ของผู้เข้าร่วมการศึกษาที่สามารถลดน้ำหนักลงได้ตั้งแต่ 5% ขึ้นไป อยู่ที่ 85%, 89% และ 91% สำหรับกลุ่มที่ได้รับ tirzepatide (Zepbound) 5 mg, 10 mg และ 15 mg ตามลำดับ เทียบกับ 35% ของกลุ่มที่ได้รับ placebo นอกจากนี้ ยังพบว่า 50% และ 57% ของกลุ่มที่ได้รับ tirzepatide (Zepbound) 10 mg และ 15 mg สามารถลดน้ำหนักลงได้ 20% หรือมากกว่า 20% ขึ้นไป เทียบกับ 3% ของกลุ่มที่ได้รับ placebo
สำหรับผลลัพธ์ของ SURMOUNT-1 ในแง่ความปลอดภัย พบว่า tirzepatide (Zepbound) มี overall safety และ tolerability profiles คล้ายคลึงกับ incretin-based therapies อื่น ๆ ที่ได้รับการรับรองจาก FDA สำหรับใช้ในการรักษาโรคอ้วน โดย adverse events ที่มีรายงานพบได้ค่อนข้างบ่อยกว่าในกลุ่มที่ได้รับ tirzepatide (Zepbound) ไม่ว่าจะเป็นขนาด 5 mg, 10 mg หรือ 15 mg เมื่อเทียบกับกลุ่มที่ได้รับ placebo ได้แก่ nausea, diarrhea, vomiting และ constipation อย่างไรก็ตาม adverse events เหล่านี้มี severity อยู่ในระดับ mild to moderate
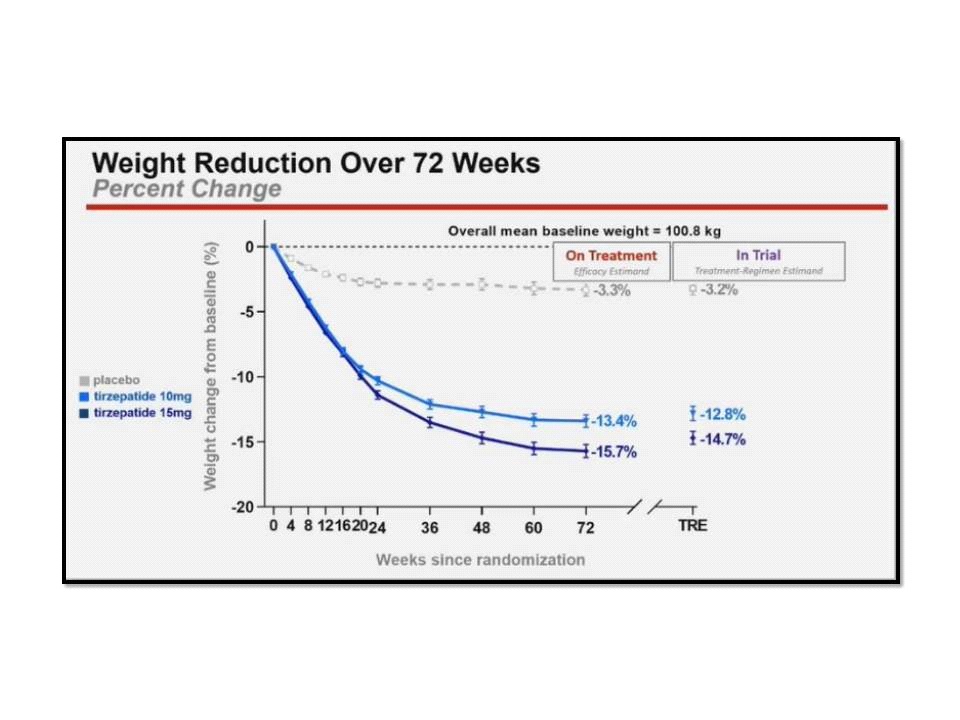
ขณะที่ SURMOUNT-2 ทำในผู้ที่มีอายุตั้งแต่ 18 ปีขึ้นไป ที่มีภาวะน้ำหนักเกิน หรือเป็นโรคอ้วน และมี weight-related condition คือ เบาหวาน ชนิดที่ 2 อยู่ด้วย จำนวน 938 คน ซึ่งถูกสุ่มแบ่งออกเป็น 3 กลุ่ม เปรียบเทียบระหว่างกลุ่มที่ได้รับ tirzepatide (Zepbound) 10 mg และ 15 mg กับกลุ่มที่ได้รับ placebo เป็นเวลา 72 สัปดาห์ โดย co-primary objectives ของการศึกษานี้ก็คือ การแสดงให้เห็นว่า tirzepatide (Zepbound) 10 mg และ 15 mg มีประสิทธิภาพเหนือกว่า placebo ทั้งในแง่ของ mean percentage change in body weight ที่ 72 สัปดาห์ จากเมื่อเริ่มต้นการศึกษา และ percentage of participants ที่สามารถลดน้ำหนักลงได้ตั้งแต่ 5% ขึ้นไป โดยเมื่อเริ่มต้นการศึกษา ผู้เข้าร่วมการศึกษานี้ส่วนใหญ่มี mean bodyweight อยู่ที่ 100.7 kg มี BMI อยู่ที่ 36.1 kg/m2 และมีระดับ HbA1c หรือค่าน้ำตาลสะสมในเลือดในช่วง 2-3 เดือนที่ผ่านมา อยู่ที่ 8.02% ผลการศึกษาของ SURMOUNT-2 ที่รายงานไว้ใน Lancet ฉบับวันที่ 19 สิงหาคม 2566 พบว่า กลุ่มที่ได้รับ tirzepatide (Zepbound) 10 mg และ 15 mg มีน้ำหนักตัวลดลงเฉลี่ยอยู่ที่ -12.8% และ -14.7% ตามลำดับ ที่ 72 สัปดาห์ จากเมื่อเริ่มต้นการศึกษา เทียบกับ -3.2% ของกลุ่มที่ได้รับ placebo ซึ่งแตกต่างกันอย่างมีนัยสำคัญทางสถิติ ขณะเดียวกันพบว่า 79–83% ของกลุ่มที่ได้รับ tirzepatide (Zepbound) 10 mg และ 15 mg สามารถลดน้ำหนักลงได้ตั้งแต่ 5% ขึ้นไป เทียบกับ 32% ของกลุ่มที่ได้รับ placebo นอกจากนี้ ยังพบว่า 39.7% และ 48.0% ของกลุ่มที่ได้รับ tirzepatide (Zepbound) 10 mg และ 15 mg ตามลำดับ ที่สามารถลดน้ำหนักลงได้ตั้งแต่ 15% ขึ้นไป ที่ 72 สัปดาห์ เทียบกับ 2.7% ของกลุ่มที่ได้รับ placebo ดังนั้น จึงเท่ากับเป็นการยืนยันว่า tirzepatide (Zepbound) 10 mg และ 15 mg มีประสิทธิภาพเหนือกว่า placebo ทั้งในแง่ของ mean percentage change in body weight ที่ 72 สัปดาห์ จากเมื่อเริ่มต้นการศึกษา และ percentage of participants ที่สามารถลดน้ำหนักลงได้ตั้งแต่ 5% ขึ้นไป
แหล่งที่มาของข้อมูล: www.fda.gov, https://investor.lilly.com, www.drugs.com, www.nejm.org, https://diabetes.medicinematters.com, www.medpagetoday.com, www2.diabetes.org