ผลการประเมินของสำนักงานอาหารและยาของสหรัฐอเมริกายืนยันว่า การใช้ยากลุ่ม GLP-1RAs ที่ได้รับการรับรองสำหรับใช้รักษาโรคเบาหวาน ชนิดที่ 2 และภาวะน้ำหนักเกิน หรือโรคอ้วน ไม่ได้มีความสัมพันธ์กับการคิดฆ่าตัวตาย ความพยายามฆ่าตัวตาย หรือการลงมือทำร้ายตัวเอง ขณะที่หน่วยงานด้านยาของสหภาพยุโรปรายงานว่า ยังไม่มีสัญญาณด้านความปลอดภัยเกี่ยวกับอุบัติการณ์ไม่พึงประสงค์ในเรื่องนี้จากการใช้ยากลุ่ม GLP-1RAs โดยเฉพาะ liraglutide และ semaglutide ที่นิยมใช้กันอย่างแพร่หลายในยุโรปสำหรับรักษาภาวะน้ำหนักเกิน หรือโรคอ้วน
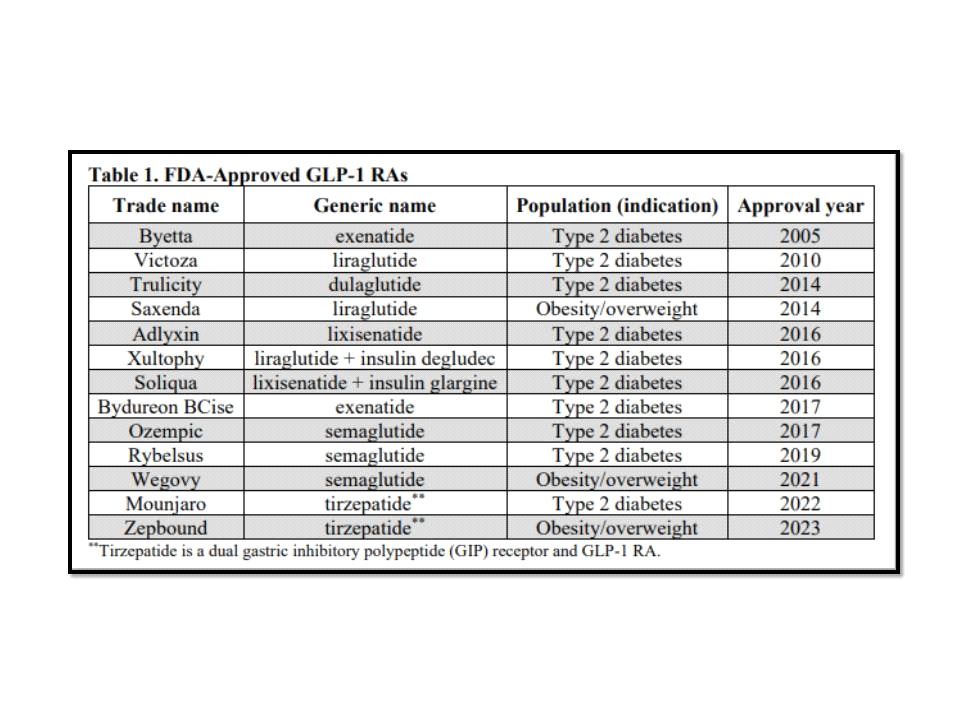
ใน Drug Safety Communication ของสำนักงานอาหารและยาของสหรัฐอเมริกา (Food and Drug Administration หรือ FDA) เมื่อวันที่ 11 มกราคม 2567 FDA รายงานว่า ในช่วงหลายเดือนที่ผ่านมา FDA ได้ทำการทบทวนรายละเอียดของรายงานเกี่ยวกับการคิดฆ่าตัวตาย หรือการฆ่าตัวตาย ของผู้ป่วยจำนวนหนึ่งที่ได้รับการรักษาด้วยยากลุ่ม glucagon-like peptide-1 receptor agonists หรือ GLP-1 RAs ที่รายงานเข้ามาผ่านทาง Adverse Event Reporting System ของ FDA หรือ FAERS โดยยากลุ่ม GLP-1 RAs ได้รับการรับรองสำหรับใช้ในการรักษาผู้ป่วยเบาหวาน ชนิดที่ 2 และมียาบางตัวในกลุ่มนี้ได้รับการรับรองสำหรับใช้ในการรักษาคนที่มีภาวะน้ำหนักเกิน หรือเป็นโรคอ้วนด้วย ผลการประเมินเบื้องต้นไม่พบหลักฐานว่าการใช้ยากลุ่มนี้ทำให้เกิดความคิดฆ่าตัวตาย หรือการฆ่าตัวตาย
Drug Safety Communication ของ FDA ระบุว่า เนื่องจากข้อมูลในเรื่องนี้ที่รายงานผ่านทาง FAERS มีค่อนข้างจำกัด และเนื่องจากความคิดฆ่าตัวตาย หรือการฆ่าตัวตาย อาจเกิดจากปัจจัยอื่น ๆ ที่มีความเป็นไปได้ ดังนั้น FDA จึงมีความเห็นว่า ข้อมูลในรายงานเกี่ยวกับความคิดฆ่าตัวตาย หรือการฆ่าตัวตาย ในผู้ป่วยจำนวนหนึ่งที่ได้รับการรักษาด้วยยากลุ่ม GLP-1 RAs ไม่ได้แสดงให้เห็นถึงความสัมพันธ์ที่ชัดเจนระหว่างการใช้ยากลุ่ม GLP-1 RAs และการเกิดความคิดฆ่าตัวตาย หรือการฆ่าตัวตาย อย่างไรก็ตาม เนื่องจากพบว่ามีความคิดฆ่าตัวตาย หรือการฆ่าตัวตาย เกิดขึ้นบ้างเล็กน้อยทั้งในกลุ่มคนที่ใช้ยากลุ่มนี้และในกลุ่มควบคุมเปรียบเทียบที่ไม่ได้ใช้ยากลุ่ม GLP-1 RAs ดังนั้น FDA จึงไม่สามารถชี้ขาดลงไปได้ว่าไม่ได้มีความเสี่ยงของความคิดฆ่าตัวตาย หรือการฆ่าตัวตาย จากการใช้ยากลุ่ม GLP-1 RAs อยู่เลย และ FDA จะยังคงติดตามเรื่องนี้ต่อไป
พร้อมกันนี้ Drug Safety Communication ของ FDA ยังแจ้งว่า FDA กำลังอยู่ระหว่างการประเมินเพิ่มเติมในเรื่องนี้ด้วยการรวบรวมและวิเคราะห์ข้อมูลด้านความปลอดภัยจากการศึกษาทางคลินิกของผลิตภัณฑ์ยาทุกตัวในกลุ่ม GLP-1 RAs รวมถึงการวิเคราะห์ข้อมูลหลังการทำการตลาดของผลิตภัณฑ์ยาทุกตัวในกลุ่ม GLP-1 RAs ใน Sentinel System ซึ่งเป็นเครือข่ายข้อมูลขนาดใหญ่ที่รวบรวบข้อมูลการใช้สิทธิประกันสุขภาพและข้อมูลผู้ป่วยที่สามารถนำมาใช้ในการสอบสวนเรื่องความปลอดภัยของผลิตภัณฑ์ยาที่ได้รับการรับรองจาก FDA
นอกจากนี้ Drug Safety Communication ของ FDA ยังมีคำแนะนำกับผู้ป่วยที่กำลังอยู่ในระหว่างการใช้ยากลุ่ม GLP-1 RAs ว่าผู้ป่วยไม่ควรหยุดการใช้ยากลุ่ม GLP-1 RAs เองโดยไม่ปรึกษาแพทย์ผู้ให้การรักษา เนื่องจากการหยุดยาเองจะทำให้อาการป่วยที่เป็นอยู่แย่ลง
การดำเนินการในเรื่องดังกล่าวของ FDA มีขึ้นหลังจากมีรายงานทั้งในสหรัฐอเมริกาและยุโรปเกี่ยวกับการคิดฆ่าตัวตาย หรือการฆ่าตัวตาย ในผู้ป่วยที่ใช้บางตัวในกลุ่ม GLP-1 RAs โดยเมื่อวันที่ 5 มกราคม 2567 สำนักข่าว Reuters รายงานว่า นับตั้งแต่ปี ค.ศ.2010 FDA ได้รับรายงานจำนวน 265 เหตุการณ์ของการคิดฆ่าตัวตาย หรือพฤติกรรมฆ่าตัวตาย ในผู้ป่วยจำนวนหนึ่งที่ใช้ยา semaglutide หรือยาในกลุ่มเดียวกัน ซึ่งในจำนวนนี้มี 36 รายงาน ที่ระบุว่าเป็นการเสียชีวิตจากการฆ่าตัวตาย หรือสงสัยว่าจะเป็นการฆ่าตัวตาย
ขณะที่ในยุโรป เมื่อวันที่ 11 กรกฎาคม 2566 PRAC (pharmacovigilance risk assessment committee) ซึ่งเป็นคณะกรรมาธิการที่มีหน้าที่ในการประเมินความเสี่ยงของผลิตภัณฑ์ยาที่ใช้กับมนุษย์ของหน่วยงานด้านยาของสหภาพยุโรป (European Medicines Agency หรือ EMA) ได้เผยแพร่รายงานการประชุมประจำวันที่ 3-6 กรกฎาคม 2566 ของ PRAC ที่ระบุว่า PRAC กำลังดำเนินการทบทวนข้อมูลเกี่ยวกับความเสี่ยงของความคิดฆ่าตัวตาย และความคิดทำร้ายตัวเองของคนที่ใช้ยากลุ่ม GLP-1 RAs ซึ่งรวมถึง semaglutide (Ozempic), liraglutide (Saxenda) และ semaglutide (Wegovy) ที่ได้รับการรับรองสำหรับรักษาโรคเบาหวาน ชนิดที่ 2 และภาวะน้ำหนักเกิน หรือโรคอ้วน หลังจากหน่วยงานด้านยาของไอซ์แลนด์ (Icelandic Medicines Agency) ได้ร้องขอให้ EMA ดำเนินการตรวจสอบในเรื่องนี้หลังจากมีรายงานเกี่ยวกับความคิดฆ่าตัวตาย หรือการทำร้ายตัวเองของคนที่ใช้ยา liraglutide และ semaglutide โดยจนถึงขณะนี้ PRAC ได้รับรายงานและกำลังอยู่ระหว่างการวิเคราะห์ข้อมูลของประมาณ 150 เหตุการณ์ ที่อาจเป็นสาเหตุของความคิดฆ่าตัวตาย หรือทำร้ายตัวเองในคนที่ใช้ยากลุ่ม GLP-1 RAs
PRAC ระบุว่า liraglutide และ semaglutide เป็นยาในกลุ่ม GLP-1 RAs ที่ปัจจุบันกำลังเป็นที่นิยมใช้กันอย่างแพร่หลายในยุโรป แต่ยังไม่เป็นที่ชัดเจนว่ารายงานเกี่ยวกับความคิดฆ่าตัวตาย หรือการทำร้ายตัวเอง ในคนที่ใช้ยา 2 ตัวนี้นั้น มีสาเหตุมาจากตัวยาเอง หรือจากโรคประจำตัวที่เป็นอยู่ หรือจากปัจจัยอื่น ๆ โดย PRAC กำลังดำเนินการทบทวนข้อมูลเกี่ยวกับสัญญาณด้านความปลอดภัยใหม่ ๆ ของยากลุ่ม GLP-1 RAs อย่างไรก็ตาม การมีสัญญาณด้านความปลอดภัยใหม่ ๆ ของยากลุ่มนี้ ไม่ได้หมายความว่ายากลุ่ม GLP-1 RAs ทำให้เกิดความคิดฆ่าตัวตาย หรือการทำร้ายตัวเอง นอกจากนี้ พฤติกรรมฆ่าตัวตายก็ไม่ได้ถูกจัดเป็น “ผลข้างเคียง” ของยาตัวใดในกลุ่ม GLP-1 RAs ที่ต้องระบุไว้ในข้อมูลผลิตภัณฑ์ยาที่ขึ้นทะเบียนและได้รับอนุมัติให้ทำการตลาดในสหภาพยุโรป
ในการประชุมครั้งหลังสุดของ PRAC ในเดือนธันวาคม 2566 EMA แจ้งว่า จนถึงขณะนี้ยังไม่สามารถหาข้อสรุปได้เกี่ยวกับความสัมพันธ์ระหว่างการใช้ยากลุ่ม GLP-1 RAs และความเสี่ยงที่จะเกิดความคิดฆ่าตัวตาย หรือการทำร้ายตัวเอง โดย PRAC ได้ขอข้อมูลเพิ่มเติมจากบรรดาบริษัทผู้ผลิตยากลุ่ม GLP-1 RAs เพราะยังมีหลายประเด็นที่ต้องทบทวนกันในรายละเอียดให้เป็นที่กระจ่างก่อนที่จะมีข้อสรุปในเรื่องนี้ออกมา โดย PRAC จะประชุมกันอีกครั้งหนึ่งในเดือนเมษายน ปี พ.ศ.2567 นี้
สำหรับข้อมูลอื่น ๆ ที่เกี่ยวข้องกับเรื่องการใช้ยากลุ่ม GLP-1 RAs และความเสี่ยงของการเกิดความคิดฆ่าตัวตาย หรือการทำร้ายตัวเองนั้น ล่าสุดมีผลการศึกษาที่น่าสนใจจากการศึกษาแบบ retrospective cohort study เรื่อง association of semaglutide with risk of suicidal ideation in a real-world cohort โดย William Wang (Center for Science, Health, and Society, Case Western Reserve University School of Medicine, Cleveland, Ohio, USA) และคณะ ที่รายงานไว้ใน Nature Medicine ฉบับวันที่ 5 มกราคม 2567 ซึ่งนำเอา electronic health records ของประชากรผู้ป่วยในสหรัฐอเมริกา จำนวน 240,618 คน จาก TriNetX Analytics Network มาวิเคราะห์ โดยผู้ป่วยเหล่านี้มีภาวะน้ำหนักเกินหรือเป็นโรคอ้วน (อายุเฉลี่ย 50 ปี, 72.6% เป็นผู้หญิง และส่วนใหญ่ 232,771 คน ไม่มีประวัติของการคิดฆ่าตัวตายมาก่อน) และได้รับการสั่งจ่ายยา semaglutide หรือยาอื่น ๆ ที่ไม่ใช่ยากลุ่ม GLP-1 RAs สำหรับการลดน้ำหนักในช่วงเดือนมิถุนายน ค.ศ.2021 ถึงเดือนธันวาคม ค.ศ.2022 โดยจากการติดตามเป็นเวลา 6 เดือน พบว่า ผู้ป่วยที่มีภาวะน้ำหนักเกิน หรือเป็นโรคอ้วน ที่ได้รับการจ่ายยา semaglutide มีความเสี่ยงของการเกิดความคิดฆ่าตัวตายน้อยกว่าอย่างมีนัยสำคัญทางสถิติ เมื่อเทียบกับกลุ่มที่ได้รับการจ่ายยาอื่นๆ ที่ไม่ใช่ยากลุ่ม GLP-1 RAs [0.11% เทียบกับ 0.43% ตามลำดับ (ต่ำกว่าเกือบ 4 เท่า); hazard ratio (HR) 0.27, 95% confident interval (CI) 0.20-0.36] ขณะเดียวกันในบรรดาผู้ป่วยที่มีภาวะน้ำหนักเกิน หรือเป็นโรคอ้วน ประมาณเกือบ 8,000 คน ที่มีประวัติของการคิดฆ่าตัวตายมาก่อน พบว่า กลุ่มที่ได้รับการจ่ายยา semaglutide มีความเสี่ยงของการเกิด recurrent suicidal thoughts น้อยกว่าอย่างมีนัยสำคัญทางสถิติ เมื่อเทียบกับกลุ่มที่ได้รับการจ่ายยาอื่น ๆ ที่ไม่ใช่ยากลุ่ม GLP-1 RAs (6.5% เทียบกับ 14.1% ตามลำดับ; HR 0.44, 95% CI 0.32-0.60)

ขณะที่อีกส่วนหนึ่งในการศึกษาเดียวกันของ William Wang และคณะ เป็นการนำเอา electronic health records ของประชากรผู้ป่วยโรคเบาหวาน ชนิดที่ 2 จำนวน 1,589,855 คน (อายุเฉลี่ย 58 ปี และ 49.2% เป็นผู้หญิง) ที่ได้รับการจ่ายยา semaglutide หรือยารักษาโรคเบาหวาน ชนิดที่ 2 ตัวอื่นๆ ที่ไม่ใช่ยากลุ่ม GLP-1 RAs ในช่วงเดือนธันวาคม ค.ศ.2017 ถึงเดือนพฤษภาคม ค.ศ.2021 จาก TriNetX Analytics Network มาวิเคราะห์ โดยผู้ป่วยเหล่านี้ส่วนใหญ่ 1,572,885 คน ไม่ได้มีประวัติของการคิดฆ่าตัวตายมาก่อน ขณะที่ผู้ป่วยอีก 16,790 คน มีประวัติของการคิดฆ่าตัวตายมาก่อน จากการติดตามเป็นเวลา 6 เดือนเช่นกัน พบว่า กลุ่มที่ได้รับการจ่ายยา semaglutide รักษาโรคเบาหวาน ชนิดที่ 2 มีความเสี่ยงของ first-time suicidal ideations อยู่ที่ 0.13% และ recurrent suicidal ideations อยู่ที่ 10% ซึ่งน้อยกว่าอย่างมีนัยสำคัญทางสถิติ เมื่อเทียบกับกลุ่มที่ได้รับการจ่ายยารักษาโรคเบาหวาน ชนิดที่ 2 ตัวอื่น ๆ ที่ไม่ใช่ยากลุ่ม GLP-1 RAs (first-time suicidal ideations 0.36% และ recurrent suicidal ideations 18%)
William Wang และคณะ สรุปว่า ผลการศึกษาของพวกเขาไม่สนับสนุนความวิตกกังวลเกี่ยวกับความสัมพันธ์ระหว่างความเสี่ยงที่เพิ่มขึ้นของการคิดฆ่าตัวตาย และการใช้ยา semaglutide ในการรักษาโรคเบาหวาน ชนิดที่ 2 และภาวะน้ำหนักเกิน หรือโรคอ้วน
แหล่งที่มาของข้อมูล: www.fda.gov, www.ema.europa.eu, www.nature.com, www.medpagetoday.com, www.tctmd.com, www.reuters.com, www.nih.gov, www.miragenews.com